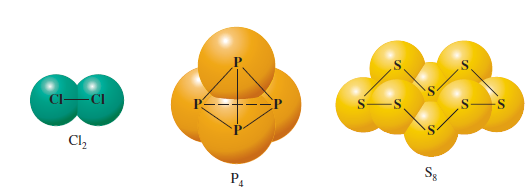
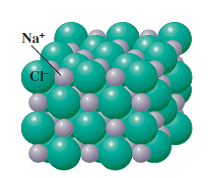
نانومتر یک واحد اندازهگیری است برابر با 9-10 متر و تمام اشیاء و موجوداتی که اندازه آنها در حد 1 تا 100 نانومتر است را نانومقیاس می نامند. خواص مواد به دو بخش خواص فیزیکی و خواص شیمیایی تقسیمبندی می شود. تجربه نشان داده ویژگیهای یک ماده خالص تا حد قابل قبولی ثابت است و این امر سبب می شود که ما بتوانیم مواد را از روی خواصشان شناسایی کنیم. اما یافتههای دانشمندان نشان میدهد که یک ماده در اندازه نانومتر ویژگیهای متفاوتی با ذرات بزرگتر خود خواهند داشت. این در حالی است که کوچک کردن ذرات، یک تغییر فیزیکی است و ما انتظار داریم که با این تغییر فیزیکی، ویژگیهای اصلی ماده تغییر نکند.
1. چرا نانو؟
1.1. چرا مقیاس نانو اهمیت دارد؟
نانومتر یک واحد اندازهگیری است برابر با 9-10 متر و تمام اشیاء و موجوداتی که اندازه آنها در حد 1 تا 100 نانومتر است، اشیاء و موجودات نانو مقیاس نامیده میشوند. این روزها نام نانو را بسیار میشنویم: علوم و فناوری نانو، دانشمندان نانو، ستاد نانو، باشگاه نانو، سمینار نانو، کارگاه نانو، کتاب نانو و ... . به نظر شما چرا این "نانو"ی بسیار کوچک اینقدر مهم شده و نامش بر سر زبانها افتاده است؟
خواص مواد را میتوان به دو بخش خواص فیزیکی و خواص شیمیایی تقسیمبندی کرد. رنگ، شفافیت، خواص الکتریکی، خواص مغناطیسی، سختی، حلالیت، نقطه ذوب و ... ویژگیهایی هستند که آنها را با نام خواص فیزیکی میشناسیم و سرعت واکنش، واکنشپذیری و .... از جمله خواص شیمیایی هستند. تجربه چند هزار ساله زندگی انسان به او نشان داده که در شرایط عادی، ویژگیهای یک ماده خاص تا حد قابل قبولی ثابت است و به این دلیل است که ما میتوانیم مواد را از روی خواصشان شناسایی کنیم.
موضوع جذابیت مقیاس نانو نیز مربوط به خواص مواد است. یافتههای دانشمندان نشان میدهد که خواص مواد در مقیاس نانو بسیار متفاوت از مقیاس ماکرو است. به عبارت دیگر اگر ذراتِ یک ماده خاص را در حد چند نانومتر (1 تا 100 نانومتر) کوچک کنیم، این ذرات ویژگیهای متفاوتی با ذرات بزرگ اولیه خواهند داشت. این در حالی است که کوچککردن ذزات یک تغییر فیزیکی است و ما انتظار نداریم که با این تغییر فیزیکی، ویژگیهای اصلی ماده تغییر کند. این امر سبب گردیده مقیاس نانو بیش از سایر مقیاسها مورد توجه قرار گیرد.
1.1.1. تغییر رنگ

شکل (1) – مقایسه ذرات شیشه خرد شده و شیشه سالم
حتما بارها خردههای یک شیشه شکسته شده را دیدهاید. ذرات حاصل از شکستن یک شیشه هر چه قدر هم که کوچک باشند، باز به بیرنگی و شفافیت شیشه اولیه هستند. اما این قاعده در مقیاس نانو صادق نیست. یعنی موادی وجود دارند که رنگ ذرات چند نانومتری آنها، با رنگ ذرات بزرگترشان متفاوت است. طلا و نقره شناخته شدهترین نمونههای این مواد هستند. شکل (2) نمودار تغییرات رنگ ذرات طلا را بر حسب اندازه آنها نشان میدهد. این پدیده در دنیای ماکرومقیاس ما یک اتفاق غیر معمول است اما از آن غیرعادیتر این است که نانو ذرات نقره با تغییر شکل هندسی هم تغییر رنگ میدهند. شکل (3) رنگ ذرات نقره و طلا را در شکلهای هندسی مختلف نشان میدهد.
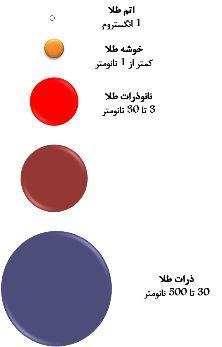
شکل (2) - رنگ ذرات طلا را بر حسب اندازه

شکل (3)- رنگ نانوذرات نقره و طلا در هندسههای مختلف
1. تغییر شفافیت
شفافیت، یک خاصیت فیزیکی است و نشاندهنده میزان توانایی یک ماده در عبود دادن نور مرئی از خود است. یک پرتو نور در برخورد با سطح ماده میتواند از آن عبور کند، جذب آن گردد یا بازتاب شود. اگر مادهای پرتوهای نور را جذب کند و یا آنها را باز تاباند، نور را مسدود کرده است. مواد مختلف بسته به عملکردشان در برابر تابش نور، میتواند کاربردهای فراوانی داشته باشد. به عنوان مثال اکسید روی و اکسید تیتانیوم نور ماورای بنفش را کاملا جذب میکنند و نور مرئی را بازتاب میکنند. این مواد که به رنگ سفید دیده میشوند، گزینههای بسیار مناسبی برای کرمهای ضد آفتاب هستند. البته افراد بسیاری رنگ سفیدی را که این کرمها بر روی پوست ایجاد میکنند، دوست ندارند. خوشبختانه این مشکل را میتوان با کوچک کردن اندازه ذرات این مواد حل کرد.
نانوذرات اکسید روی و اکسید تیتانیوم، با وجود اینکه نور ماورای بنفش را کاملا جذب میکنند، اما برخلاف ذرات بزرگتر کاملا شفاف هستند. البته این امر ناشی از عبور نور مرئی از این ذرات نیست، بلکه به سبب آن است که اندازه نانوذرات اکسید روی و اکسید تیتانیوم کوچکتر از طول موج نور مرئی (400-700 نانومتر) است و از این رو این ذرات توانایی بازتابش نور مرئی را ندارند.

شکل (4)– تغییر رنگ ذرات اکسید تیتانیوم بر حسب اندازه
3.1.1. تغییر خواص مغناطیسی
کمی براده آهن را در یک لیوان آب حل کنید و آن را خوب به هم بزنید. قبل از اینکه برادهها تهنشین شوند، یک آهنربا را به لیوان نزدیک کنید. چه اتفاقی میافتد؟ آیا مخلوط آب و براده نسبت به میدان مغناطیسی آهنربا عکسالعملی نشان میدهد؟ اگر این آزمایش را خیلی خوب انجام داده باشید، بهترین نتیجه حاصل جذب ذرات براده توسط آهنربا است. اما اگر همین آزمایش را توسط ذرات نانومتری آهن (یا کبالت) تکرار کنیم، نتیجه متفاوت خواهد بود.
سیال مغناطیسی (یا فروفلوید) مایعی است متشکل از نانوذرات فرومغناطیس (مانند آهن و کبالت) که در آب یا یک حلال آلی معلق شدهاند. این مایع در حضور یک آهنربا (یک میدان مغناطیسی) خاصیت مغنایسی بسیار قوی از خود نشان میدهد، به نحوی که با حرکت آهنربا در اطراف این مایع میتوان آن را به شکلهای سهبعدی زیبایی درآورد. البته این سیال تا زمانی از خود چنین خاصیتی نشان میدهد که ذرات نانومتری آن (تحت نیروهای بینمولکولی) به یکدیگر نچسبند.

شکل (5)- سیال مغناطیسی
4.1.1. تغییر واکنشپذیری
خواص شیمیایی یک ماده، خواصی هستند که به طور مستقل نمیتوان آنها را اندازهگیری کرد. به این معنا که مقدار یک کمیت شیمیایی در طی واکنش و برهمکنش یک ماده با مواد دیگر مشخص میشود. واکنشپذیری یا تمایل یک ماده برای واکنش با سایر مواد، از جمله مهمترین خواص شیمیایی است. بیشتر ما صحنه شعلهور شدن سدیم، لیتیم یا پتاسیم را در تماس با آب دیدهایم (شکل 6). همه این ها عناصری هستند که به شدت واکنشپذیرند. تا آنجا که نمیتوان آنها را مانند سایر عناصر در تماس با هوا نگه داشت. اما در مقابل با انداختن یک انگشتر طلا در یک لیوان آب اتفاقی نمیافتد و یا پنجرههای آلومینیومی بدون هرگونه مشکلی در مجاورت هوا استفاده میشوند (البته این به مدد لایه مقاوم اکسیدی است که بر روی سطح آلومینیوم تشکیل میشود). اما همین مواد در مقیاس نانو رفتار متفاوتی از خود نشان میدهند.

شکل (6)- واکنشپذیری بالای سدیم و آب
واکنشپذیری مواد در مقیاس نانو افزایش چشمگیری پیدا میکند. در این مقیاس ذرات طلا نه تنها واکنشپذیری بالایی دارند، بلکه برای افزایش سرعت واکنش مواد دیگر (به عنوان کاتالیزگر) نیز استفاده میشوند. نانوذرات آلومینیوم در هوا آتش میگیرند و میتوان از آنها به عنوان سوخت موشک استفاده کرد. افزایش واکنشپذیری مواد در این مقیاس، امکان ساخت کاتالیزگرهای بسیار قویتری را برای ما فراهم کرده است. تا آنجا که پیشبینی میشود بتوانیم با استفاده از نانوکاتالیزگرها واکنشهای بازگشتناپذیر بسیاری را (مانند تشکیل گازهای سمی NO و CO) در دما و فشار محیط برگشتپذیر کنیم.
آنچه گفته شد تنها مثالهای محدودی از تغییر ویژگیهای یک ماده در مقیاس نانو است. نقطه ذوب، خواص حرارتی، خواص الکتریکی، خواص مکانیکی و دهها خاصیت فیزیکی و شیمیایی شناخته شده دیگر نیز در این مقیاس تغییر میکنند. گویا دیگر نمیتوانیم بدون در نظر گرفتن اندازه ذرات یک ماده، آنرا از روی خواصش شناسایی کنیم. برخی برای حل این مشکل پیشنهاد دادهاند که یک بُعد دیگر به جدول تناولی مندلیف اضافه کنیم. بدین معنی که برای مشخص کردن خواص یک عنصر، علاوه بر اینکه باید نام آن عنصر و جایگاه آن را در جدول مندلیف مشخص کنیم، لازم است که معلوم کنیم خواص عنصر را در چه ابعادی میخواهیم.
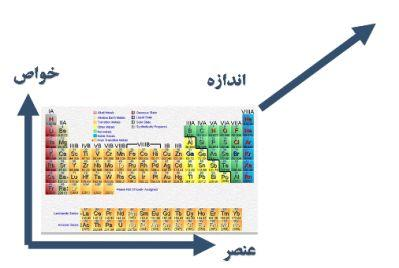
شکل(7)- جدول تناوبی سه بعدی
ما در دنیای ماکرومقیاس اطرافمان، مواد را با توجه به خواصشان دستهبندی میکنیم و سپس متناسب با این خواص، آنها را برای انجام کارهای مختلف انتخاب میکنیم. برای ساخت پنجره از شیشه استفاده میکنیم، زیرا شفاف است و نور را از خود عبور میدهد؛ برای ساخت زیورآلات ماندگار از طلا استفاده میکنیم، زیرا واکنشپذیری پایینی دارد و اکسید نمیشود؛ برق را با رشتههای مسی انتقال میدهیم چرا که پس از طلا و نقره بیشترین ضریب انتقال الکتریکی را در بین عناصر مختلف دارد و از آنجا که فولاد یکی از سختترین مواد دنیای ماست، ابزارهای بزرگی صنعتیمان را از آن میسازیم.
http://edu.nano.ir